根據(jù)題目描述,某同學(xué)采用一套實驗裝置研究物質(zhì)(特別是氯氣)的性質(zhì)。氣體c的主要成分是氯氣(Cl?),同時含有少量空氣和水蒸氣。這種混合氣體在化學(xué)實驗中具有典型性,常被用于探究氯氣的化學(xué)性質(zhì),尤其是其強(qiáng)氧化性、與水反應(yīng)以及與堿反應(yīng)等特性。
一、 實驗裝置與氣體c的組成分析
- 氣體來源:氯氣通常通過濃鹽酸與二氧化錳(MnO?)加熱制備,或用高錳酸鉀(KMnO?)與濃鹽酸常溫反應(yīng)制得。在制備過程中,難以完全排盡裝置內(nèi)的空氣,且鹽酸具有揮發(fā)性,生成的氯氣也常帶有水蒸氣,因此得到的氣體c是含有少量空氣和水蒸氣的氯氣混合物。
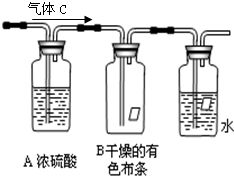
- 裝置作用:完整的實驗裝置通常包括氣體發(fā)生裝置、凈化干燥裝置、性質(zhì)探究主體裝置以及尾氣處理裝置。針對氣體c含有雜質(zhì)的特點,可能需要在主體反應(yīng)前連接干燥裝置(如濃硫酸洗氣瓶)以除去水蒸氣,防止干擾后續(xù)反應(yīng)。空氣的存在(主要是O?和N?)在多數(shù)氯氣性質(zhì)實驗中影響相對較小,但若進(jìn)行非常精確的定量研究或涉及催化反應(yīng)時需考慮。
二、 氯氣(主體)性質(zhì)探究要點
將這種混合氣體通入不同試劑,可以系統(tǒng)性研究氯氣的核心化學(xué)性質(zhì):
1. 漂白性與次氯酸(HClO)的生成:將氣體c通入濕潤的有色布條或品紅溶液,布條或溶液褪色,證明氯氣與水反應(yīng)生成的次氯酸(HClO)具有漂白性:
Cl? + H?O ? HCl + HClO
而干燥的氯氣本身不具備漂白性,通過對比實驗可清晰證明。混合氣體中的水蒸氣恰好為此反應(yīng)提供了條件。
- 強(qiáng)氧化性:
- 與金屬反應(yīng):將氣體c通入裝有灼熱銅絲或鐵粉的硬質(zhì)玻璃管,可觀察到生成棕黃色的煙(CuCl?顆粒)或棕褐色煙(FeCl?顆粒),證明氯氣能與大多數(shù)金屬化合生成高價金屬氯化物。
- 與還原性物質(zhì)反應(yīng):通入硫化氫(H?S)溶液,溶液變渾濁(生成硫單質(zhì)沉淀);通入碘化鉀(KI)溶液,溶液顏色變深(生成碘單質(zhì),I?溶于水呈棕黃色)。
* 與堿反應(yīng):通入氫氧化鈉(NaOH)溶液,發(fā)生反應(yīng)生成次氯酸鈉(NaClO)和氯化鈉(NaCl),這是工業(yè)制漂白液的原理,也是實驗中吸收尾氣、防止污染的關(guān)鍵反應(yīng):
Cl? + 2NaOH → NaCl + NaClO + H?O
三、 雜質(zhì)的影響與實驗注意事項
- 水蒸氣的影響:水蒸氣的存在是一把“雙刃劍”。一方面,它使氯氣能表現(xiàn)其漂白性;另一方面,若研究干燥氯氣的性質(zhì)(如與干燥金屬反應(yīng)),它可能成為干擾因素。潮濕的氯氣腐蝕性更強(qiáng),對裝置氣密性和材料(如橡膠管)要求更高。
- 空氣的影響:少量空氣中的氧氣在常溫下與氯氣共存時,通常不干擾氯氣的主體反應(yīng)。但在涉及高溫反應(yīng)時需注意安全。空氣的存在也意味著氣體c并非純凈物,在需要精確計量氣體體積或進(jìn)行定量分析時,需要通過排飽和食鹽水法收集純氯氣。
- 安全與環(huán)保:氯氣有毒,任何涉及氯氣的實驗都必須在通風(fēng)櫥內(nèi)進(jìn)行,或確保裝置密閉且配有有效的尾氣吸收裝置(通常用NaOH溶液)。實驗結(jié)束后,裝置內(nèi)殘余的氯氣也需用堿液充分吸收處理。
結(jié)論:
研究以氯氣為主要成分,并含有少量空氣和水蒸氣的氣體c的性質(zhì),是一個經(jīng)典的綜合實驗。它不僅能系統(tǒng)驗證氯氣的漂白性、強(qiáng)氧化性等核心化學(xué)性質(zhì),還能讓學(xué)生理解氣體凈化、雜質(zhì)影響、對比實驗設(shè)計和尾氣處理等重要的實驗方法論與安全理念。實驗的關(guān)鍵在于根據(jù)具體探究目標(biāo),合理設(shè)計裝置順序(如是否干燥),設(shè)置對照實驗,并始終將安全操作放在首位。